2018年肝细胞扩增基础研究重大突破
发布时间:2018-11-29 10:11:29
2018年9月,第二军医大学,以王阳红院士为首的科研团队成功实现了体外肝细胞的高效扩增,可实现肝细胞体外扩增10代以上。扩增后的肝细胞经过诱导培养基诱导后,肝细胞支持HBV感染,说明肝细胞的分化状态相对较高。将诱导后的肝细胞注射到免疫缺陷的FAH-/-小鼠中,可以治愈小鼠的遗传性高酪氨酸血症,并且可以实现人肝细胞的高度嵌合生长。该项研究结果发表在亚洲最高影响因子的Cell Research上(https://doi.org/10.1038/s41422-018-0103-x),代表性结果如下:
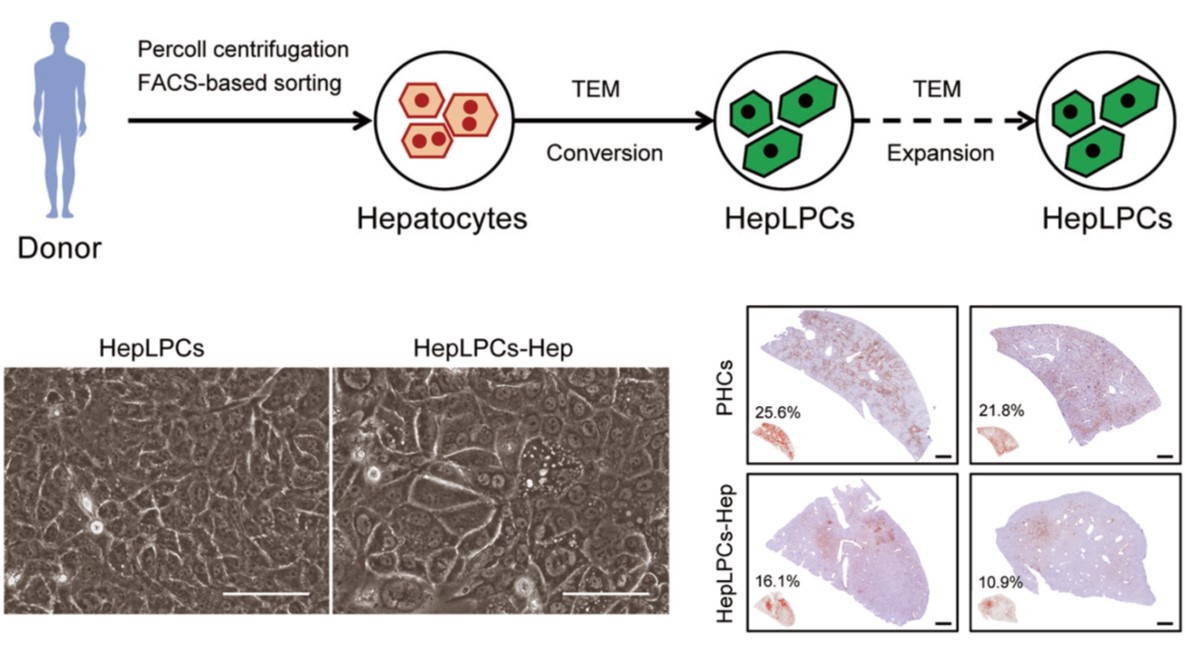
无独有偶,中科院上海生物化学与细胞生物学研究所的惠利健团队也报道了体外高效扩增人肝细胞的方法,相关结果发表在Cell子刊《Cell stem cell》(https://doi.org/10.1016/j.stem.2018.10.018)。
两个独立平行研究同时发表在顶尖学术期刊上,说明了该项研究的重要性。我国是肝病大国,特别是乙肝病毒感染率达7.8%。原代肝细胞主要有三个临床应用场景。场景一:原位肝移植等待供体肝的生命搭桥,每年我国约有40万病人需要进行肝移植,实际实施肝移植的病人仅约4000例,约90%的病人在等待供体肝的过程中死去;通过肝细胞移植可以延长病人的等待时间,直到成功进行肝移植。场景二:我国每年新发急慢性肝衰病例超过100万例,大部分病人依赖传统的治疗策略,治疗效果差,多发死亡病例;利用原代肝细胞制备成“生物人工肝”,与体内肝细胞的生理功能最接近,治疗效果理论上更好,有望迭代传统治疗策略。场景三:中国人口基数大,肝脏代谢遗传病种类繁多,包括A尿素循环的先天缺陷(致命,发病率1:3万至1:10万)、Crigler–Najjar综合征I型(致命, 1:10万)、糖原贮积病Ⅰ型(可致死,1:10万至1:30万)、因子VII缺乏[症](凝血异常,极少见)、家族性高胆固醇血症(心血管疾病,发病率高达1/ 500)、遗传性酪氨酸血症I型,FAH 基因缺陷所致(肝功能衰竭、肝硬化和肝细胞癌(HCC),发病6.7:10万)等等,利用原代肝细胞移植治疗肝脏遗传代谢病在国外是成熟的治疗手段,取得了不错的治疗效果。
目前的研究进展已经回答了0到1的问题,然而由于细胞体外扩增成本太“烧钱”,此项技术的临床应用还有一定的距离。相信在不远的将来,通过科学家和企业家的不懈努力,我们终将攻克肝脏顽疾。

