原代细胞冻存
详述
1 人原代肝细胞、胰岛细胞用途
人原代肝细胞是指从肝组织取出后立即培养或者冻存的肝细胞,是一种“金标准”细胞模型,可广泛用于基础研究与药物研发,包括肝脏研究、肝炎病毒研究,药物代谢及毒性研究。CFDA在《药物非临床药代动力学研究技术指导原则》中明确,原代肝细胞是体外小分子、中药提取物等药物评价的重要细胞模型。目前,基于原代肝细胞和肝非实质细胞开发的类器官/圆球体、肝脏芯片等技术是未来新药研发与评价的发展趋势。同时,原代肝细胞作为肝功能的主要扮演者,可用于安全而有效的细胞治疗和生物人工肝,包括原位肝移植的“生命搭桥”、治疗急性肝功能衰竭、治疗肝脏代谢遗传病等。原代肝细胞具有众多的技术瓶颈,包括批次差异大、分离与冻存难、培养时间短等,这严重限制了人原代肝细胞的应用。
人胰岛是指胰腺器官中的发挥调控血糖变化的内分泌细胞团,主要包含四类细胞,α细胞、β细胞、δ细胞和PP细胞。胰岛PP细胞在胰岛细胞中占比最小,约为1%,分泌胰多肽;δ细胞约占6%~15%,分泌生长抑素;α细胞占24%~40%,分泌胰高血糖素;β细胞占比最大,为60%~80%,分泌胰岛素。胰高血糖素和胰岛素是调控人体血糖变化最为关键的两种内分泌激素:胰高血糖素能够升高人血液中的葡萄糖含量,以保证人体产生足够的热量维持机能;胰岛素则相反,能够降低血糖浓度,促进血液中的葡萄糖转运到肝脏和肌肉中合成糖原贮存。分离与保藏胰岛细胞可用于基础科学研究,包括药物的毒理研究、内分泌研究、糖尿病机理研究、糖尿病治疗研究等;更重要的是,结合3D生物打印技术或者胰岛团体外重构技术,最终运用到临床以根治1型糖尿病。
2细胞来源
目前,人原代肝/胰岛细胞主要从临床上捐献材料包括遗体捐献、手术切除样本中获取等,这些临床样本具有最原始的生理与疾病相关性,具有重要的基础研究与临床治疗价值。肝组织材料主要分为以下3类:1)成人供体肝:通常情况下,临床捐献用于移植的肝脏存在一定概率不能用于肝移植的特殊情形,包括但不限于器官离体时间太长、受体情况提前恶化或者死亡、手术失败等;2)劈离式肝移植:由于供体肝体积过大,肝脏需要经过手术修整后以适合更小(儿童)体型,这样将产生较大体积肝脏废弃物;3)其他类型的疾病肝组织,如血管瘤、胆道闭锁等问题需要切除肝脏或者肝组织的。胰岛材料主要包括:1)成人胰腺供体:临床上,供体胰腺直接移植到1型糖尿病患者体内的移植手术开展规模很小,而将胰腺中的胰岛分离纯化出来再移植到患者肝内的胰岛移植手术,具有副作用小、微创、安全有效等优点,更受医疗工作者青睐。然而,受制于国内胰岛分离纯化技术的团队严重不足,临床上绝大部分胰腺供体尚不能用于糖尿病治疗;2)急性胰腺炎患者的胰腺:药物治疗效果不理想、反复发作的急性胰腺炎患者,只能选择手术切除胰腺。
以上肝脏、胰腺捐献材料,在征得病人家属知情同意、符合伦理要求的情况下,通常情况下用于教学、科学研究或者作为医疗垃圾进行无害化处理。由于医院缺乏专业化分离保藏技术,包括大规模分离、高效冻存与复苏技术,大部分医院只能做简单的取材或者直接无害化处理。因此,临床肝组织、胰腺材料的这些宝贵的人类遗传资源需要进行合理有效的资源保藏与利用,以满足我国基础研究和临床治疗对肝细胞、胰岛细胞日益增长的需求。
3 人原代肝细胞、胰岛细胞冻存的必要性
人原代肝细胞冻存的必要性主要包括:1)为治疗急性肝衰竭提供研究素材和细胞来源,我国每年有100万新发急性肝衰竭病例,基于原代肝细胞的细胞治疗、生物人工肝等新方法和治疗产品可以解决目前的重大临床需求,具有巨大的临床转化前景; 2)人遗资源变“废”为“宝”,医院用于简单取材、无害化处理的医疗废弃物,通过我司在原代肝细胞领域的技术积累,可以对肝细胞进行分规模化分离与冻存,建立活细胞库,实现人肝组织变“废”为“宝”,满足临床治疗与科学研究的需要;3)便于长期储存与长距离运输,可通过液氮对细胞进行长期储存,根据医务工作者或者科研工作者的实际需求通过干冰或液氮进行长距离转运;4)为中国新药研发提供最佳测试模型,药物CYP代谢酶因人种不同而存在巨大差异,适用于中国人的药物的最佳药物代谢细胞模型是具有中国遗传背景的原代肝细胞,如中美两国关于瑞德西韦(Remdesivir)治疗新冠病毒,可能原因是中国人对瑞德西韦的代谢与清除与美国人存在人种差异;6)打破技术封锁,原代肝细胞的冻存与复苏技术是极其重要的技术瓶颈,我国长期受到欧美发达国家的技术封锁,导致我国在生物医药研发的关键原料上长期依赖进口,且价格昂贵,大量纳税人的钱进入外国人口袋。
胰岛细胞冻存的必要性主要包括:1)提高供体材料的有效利用,目前我国掌握人胰岛细胞分离技术的团队不足,临床上较为丰富的供体胰腺与巨大的I型糖尿病病人数形成鲜明的供需失衡,造成了的极大浪费;2)糖尿病治疗的迫切需要,我国仅I型糖尿病病人数就约600-1000万之多,胰岛移植作为根治I型糖尿病的安全方法,移植物平均生存时间长达9.8年,避免胰岛素注射造成的实质器官不可逆损伤,提升I性糖尿病生活质量并降低其医疗负担;3)提升细胞得率与胰岛冻存活力,目前关于胰岛的分离与冻存都只限于胰岛细胞团的整体分离与冻存,单个细胞被认为是没有功能的,这降低了细胞得率;另一方面,胰岛是个细胞团,处于细胞团内部的细胞由于冻存液渗透和受热不均等原因,冻存和复苏的效果很差;我们将纯化的胰岛细胞团酶解成胰岛单细胞,进行细胞冻存和复苏,复苏后胰岛单细胞在体外重构形成有内分泌功能的细胞团(胰岛),提升了细胞得率与胰岛冻存活力;4)提高胰岛细胞的可及性,我公司的分离与冻存技术能很好的解决1型糖尿病患者与胰腺供体之间时空距离问题,同时解决患者一次移植效果不佳时的二次甚至多次移植需求。
相关文章发表
Revival, characterization, and hepatitis B virus infection of cryopreserved human fetal hepatocytes.
Zhou M, Huang Y, Cheng Z, Zhao F, Li J, Zhi X, Tian X, Sun W, Hu K.
J Virol Methods. 2014 Oct;207:29-37. doi: 10.1016/j.jviromet.2014.06.015. Epub 2014 Jun 28.
PMID: 24977316
Primary human hepatocytes are considered the ideal cellular model for in-vitro studies of liver-specific pathology, such as hepatitis B virus (HBV) infection. ...Moreover, this optimized model was susceptible to HBV infection and could be used to screen entry inhibi …

肝细胞再生
详述
我国是一个肝病大国。据保守估计,肝病人数高达4亿,其中乙肝病毒感染者约9300万,丙肝病毒感染者1300万,酒精性脂肪肝6000万,非酒精性脂肪肝2亿。庞大的患者基数,严重降低了我国人口素质、增加了国家经济负担,制约着我国向发达国家行列迈进的步伐。彻底改善我国肝病现状成为人民公仆迫切想解决的问题,通过加大肝病基础研究与新药研发的支持力度,这使得我国成为当今世界肝病研究与进展最活跃的国家之一。原代肝细胞作为一种细胞模型,在肝病基础研究与新药研发中发挥着无可替代的作用。同时,原代肝细胞作为一种肝功能生命载体,在肝细胞移植、生物人工肝以及肝脏器官3D打印等医疗领域具有重要的应用价值。
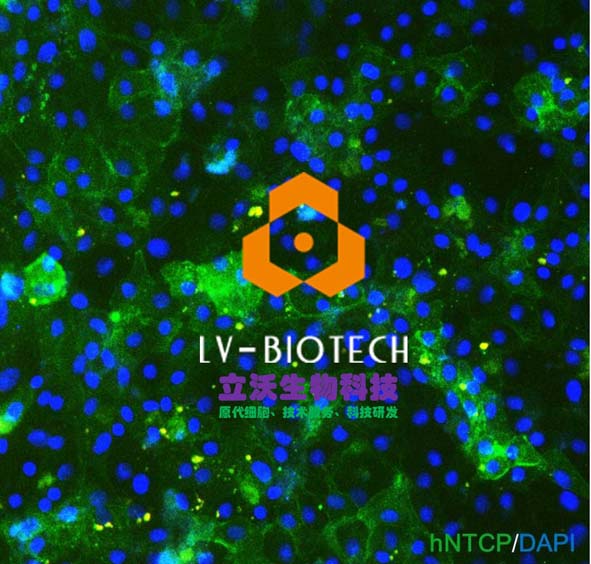
原代肝细胞是指从机体内取出后立即培养的肝细胞,相对于传统肝癌或者永生化细胞系,具有高度分化的特性,最接近体内真实的细胞环境,是肝脏代谢、肝脏疾病、肝炎病毒等领域的“金标准”细胞模型。FDA及CFDA规定,在《药物非临床药代动力学研究的技术指导原则》中,明确了人原代肝细胞及其附属产品在药物研发当中的重要性。原代肝细胞,具有完整的药物吸收与代谢体系,包括药物转运(如NTCP)、毒性(如MPR2等)、代谢(如CYP450系列酶)相关的酶,最能反映细胞对药物的真实反应。特别是,不同人种的药物代谢相关基因表达水平差异极大,研发针对中国人的药物需要具有中国遗传背景的原代肝细胞,以获得准确的药物安全性数据。因此,原代肝细胞及其附属产品作为新药研发过程中的刚需,助力于我国生物医药的快速发展。
人原代肝细胞是肝功能最小的生命单位,具有重要的临床应用价值。原代肝细胞主要包括三个临床应用场景。场景一:原位肝移植等待供体肝的“生命搭桥”,每年我国约有40万病人需要进行肝移植,实际实施肝移植的病人仅约4000例,约90%的病人在等待供体肝的过程中死去;通过肝细胞移植可以有效地延长病人的等待时间,直到成功进行肝移植。场景二:我国每年新发急慢性肝衰病例超过100万例,大部分病人依赖传统的人工肝,治疗效果差,多发死亡病例;利用原代肝细胞制备成“生物人工肝”,与体内肝细胞的生理功能最接近,治疗效果理论上更好,有望迭代传统人工肝。场景三:通过肝细胞会输治疗肝脏代谢遗传病;中国人口基数大,肝脏代谢遗传病种类繁多,包括A 尿素循环的先天缺陷(致命,发病率1:3万至1:10万)、Crigler–Najjar综合征I型(致命, 1:10万)、糖原贮积病Ⅰ型(可致死,1:10万至1:30万)、因子VII缺乏[症](凝血异常,极少见)、家族性高胆固醇血症(心血管疾病,发病率高达1/ 500)、遗传性酪氨酸血症I型,FAH 基因缺陷所致(肝功能衰竭、肝硬化和肝细胞癌(HCC),发病6.7:10万)等等。在国外,利用原代肝细胞进行肝移植生命搭桥、治疗急慢性肝功能衰竭、治疗肝脏遗传代谢病是成熟的治疗手段,国内仅解放军302医院做过并报道了相关临床试验,绝大部分病例都显示肝细胞移植的安全性和有效性。
基于FAH基因缺陷大鼠模型的人肝细胞扩增技术是解决人原代肝细胞来源问题的必要手段。目前,人原代肝细胞主要来源于人体捐献材料、手术切除肝组织等。由于亚洲文化差异、医学伦理、法律法规等问题,人原代肝细胞的获取存很大的难度。本项目拟开发的技术有望彻底解决人原代肝细胞来源问题,规避严重的医学伦理问题。基于动物模型的人肝细胞扩增或再生技术是人原代肝细胞标准化生产的重要途径。人原代肝细胞具有较大的批次差异,特别是药物代谢相关的CYP基因,人种差异上十倍,个体差异可达千倍,因此用于药物代谢测试的人原代肝细胞需要多个供体混合在一起。尽管这样,当某些批次的人原代肝细胞用完之后,任然需要新的批次的混合细胞,新的批次混合的肝细胞相较于上一批次的细胞存在无法避免的较大差异。基于FAH基因缺陷大鼠模型的人肝细胞扩增技术,理论上可以获得源源不断的人肝细胞供应,多个供体的人原代肝细胞可以混合移植或者单独移植,从而建立标准的、稳定的人原代肝细胞产品,有望成为行业内的“行业标准”。
相关文章发表
胰岛细胞再生
详述
人胰岛是指胰腺器官中的发挥调控血糖变化的内分泌细胞团,主要包含四类细胞,α细胞、β细胞、δ细胞和PP细胞。胰岛PP细胞在胰岛细胞中占比最小,约为1%,分泌胰多肽;δ细胞约占6%~15%,分泌生长抑素;α细胞占24%~40%,分泌胰高血糖素;β细胞占比最大,为60%~80%,分泌胰岛素。胰高血糖素和胰岛素是调控人体血糖变化最为关键的两种内分泌激素:胰高血糖素能够升高人血液中的葡萄糖含量,以保证人体产生足够的热量维持机能;胰岛素则相反,能够降低血糖浓度,促进血液中的葡萄糖转运到肝脏和肌肉中合成糖原贮存。分离与保藏胰岛细胞可用于基础科学研究,包括药物的毒理研究、内分泌研究、糖尿病机理研究、糖尿病治疗研究等;更重要的是,结合3D生物打印技术或者胰岛团体外重构技术,最终运用到临床以根治1型糖尿病。
然而,胰岛细胞主要来源于临床捐献,主要包括:1)成人胰腺供体:临床上,供体胰腺直接移植到1型糖尿病患者体内的移植手术开展规模很小,而将胰腺中的胰岛分离纯化出来再移植到患者肝内的胰岛移植手术,具有副作用小、微创、安全有效等优点,更受医疗工作者青睐。然而,受制于国内胰岛分离纯化技术的团队严重不足,临床上绝大部分胰腺供体尚不能用于糖尿病治疗;2)急性胰腺炎患者的胰腺:药物治疗效果不理想、反复发作的急性胰腺炎患者,只能选择手术切除胰腺。主要问题:1)来源有限,2)伦理问题,3)批次差异。因此,如何再生胰岛细胞成为该领域的重要研究方向。
相关文章发表




